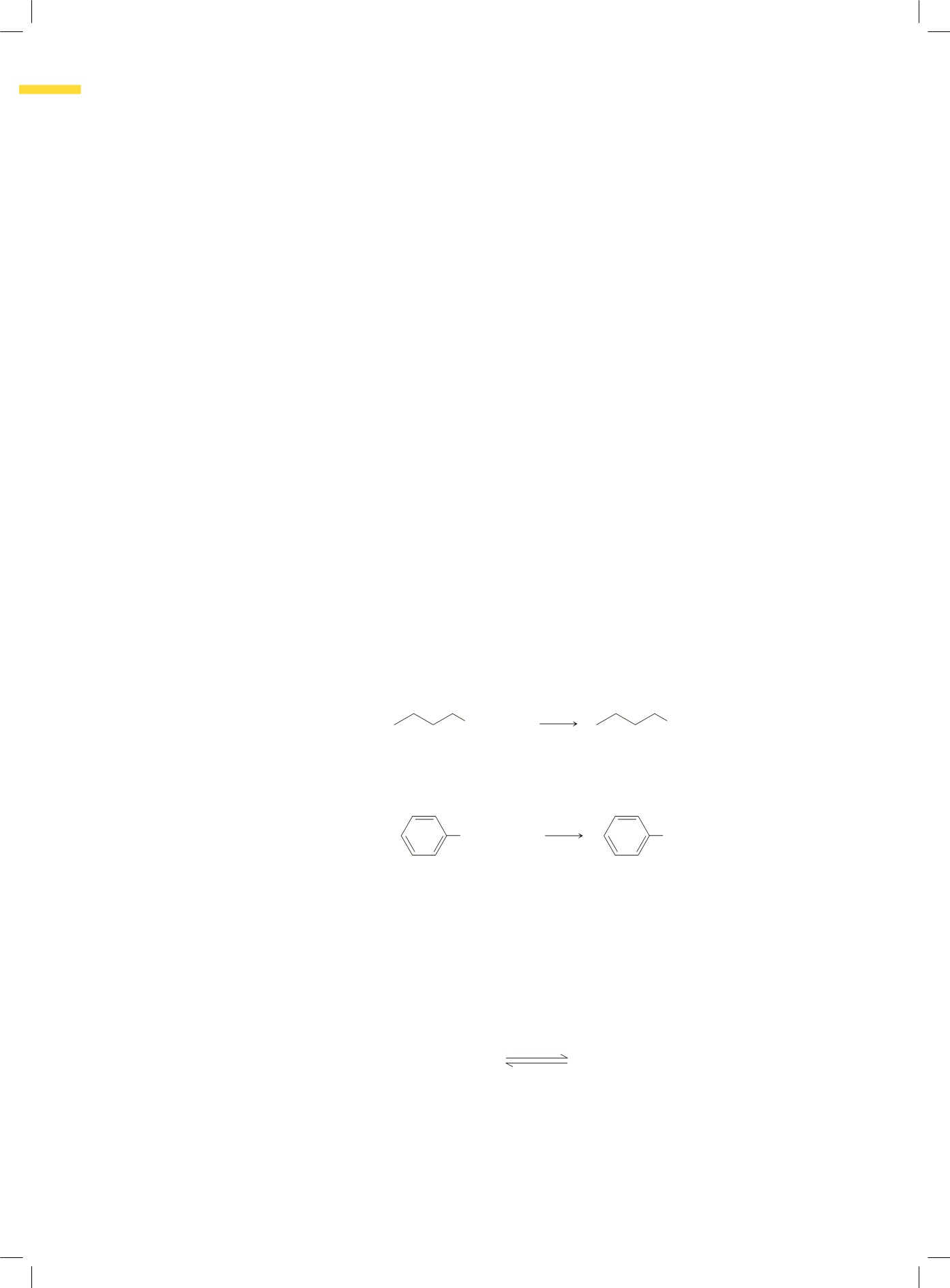
Capitolo 12
Un’introduzione
ai composti
organometallici
492
basiche. Successivamente discuteremo più dettagliatamente del loro uso nella sintesi
organica, in particolare nei Capitoli 13 e 15.
RMgX
RLi
Un composto organometallico
Un composto organometallico
del magnesio
del litio
(un reattivo di Grignard)
A. Preparazione e struttura
I composti organomagnesiaci sono tra i composti organometallici più facilmente
disponibili, preparabili e maneggevoli. Sono comunemente noti come reattivi di
Grignard, dal nome del chimico francese Victor Grignard (1871-1935), che è stato
insignito del Premio Nobel per la Chimica proprio per la scoperta di tali reattivi e la
loro utilizzazione in sintesi organica.
I reattivi di Grignard vengono solitamente preparati per lenta addizione di un
alogenuro alchilico, arilico o alchenilico (vinilico) ad una sospensione, tenuta sotto
agitazione, di magnesio metallico, in leggero eccesso, in un solvente etereo, di solito
etere dietilico o tetraidrofurano (THF). Gli ioduri ed i bromuri organici di solito rea-
giscono molto rapidamente in queste condizioni, laddove la maggior parte dei cloruri
organici è più lenta a reagire. I bromuri sono i più comuni materiali di partenza per la
preparazione dei reattivi di Grignard. Qualora per la preparazione dei reattivi di Gri-
gnard vengano impiegati alogenuri organici più lenti a reagire, si utilizza THF quale
solvente
(p.e. 67°C)
. La reazione è caratterizzata da un periodo di induzione causato
dalla presenza di tracce di umidità e dalla presenza di un sottile strato di ossido sulla
superficie del magnesio. Quando la reazione è innescata, è esotermica e il rimanente
alogenuro alchilico viene aggiunto in piccole quantità sufficienti a mantenere un ri-
flusso moderato del solvente etereo.
Il bromuro di butilmagnesio, ad esempio, viene preparato per trattamento
dell’1-bromobutano con magnesio metallico in etere dietilico. I reattivi arilici di Gri-
gnard, come il bromuro di fenilmagnesio, vengono preparati secondo la stessa proce-
dura. Queste reazioni sono addizioni ossidative, in cui il magnesio passa dallo stato
Mg(0)
allo stato
Mg(II)
.
etere
Br Mg
MgBr
1-Bromobutano
Bromuro di butilmagnesio
(un reattivo di Grignard alchilico)
1
Br
MgBr
Bromobenzene
Bromuro di fenilmagnesio
(un reattivo di Grignard arilico)
etere
Mg
1
Sebbene l’equazione di formazione dei reattivi di Grignard si dimostri semplice, il
meccanismo è considerevolmente più complicato e coinvolge radicali. La discussione
di tale meccanismo non è necessaria a questo livello. Comunque, è da sottolineare
che per molti reattivi di Grignard esiste un equilibrio tra i complessi monoalchilma-
gnesiaco e dialchilmagnesiaco, come di seguito riportato.
2 RMgX
R
2
Mg
1
MgX
2
I reattivi di Grignard si formano sulla superficie del metallo e passano in solu-
zione come complessi di coordinazione solvatati dall’etere. In tale complesso solubile
in etere, il magnesio si comporta da acido di Lewis, mentre l’etere si comporta da
base di Lewis (Figura 12.1).