
92
C A P I T O L O 4
Conduttori. Dielettrici. Energia elettrostatica
POLARIZZAZIONE DEI DIELETTRICI
La spiegazione dei fenomeni osservati si basa sulla struttura elettrica microsco-
pica della materia. Ricordiamo come il fenomeno dell’induzione elettrostatica,
che rende possibile la separazione delle cariche dei due segni nei conduttori, sia
dovuto al fatto che nei conduttori un certo numero di elettroni per atomo è sepa-
rato dall’atomo stesso: all’interno dei conduttori esiste un
gas di elettroni
pratica-
mente liberi.
Negli isolanti invece tutti gli elettroni sono legati agli atomi e non se ne allon-
tanano spontaneamente. Per fare avvenire la separazione occorre agire
dall’esterno, ad esempio tramite lo strofinio con un panno. Se si applica al dielet-
trico un campo elettrico esterno avviene soltanto uno
spostamento locale
delle cari-
che che costituiscono gli atomi. Si tratta di effetti molto piccoli per ogni singolo
atomo: gli spostamenti delle cariche sono dell’ordine di 10
–15
m, confrontabili con
le dimensioni del nucleo. Però il numero di atomi per unità di volume è
n
= 10
25
÷
10
28
m
–3
, a seconda dello stato di aggregazione, per cui l’effetto complessivo è mi-
surabile.
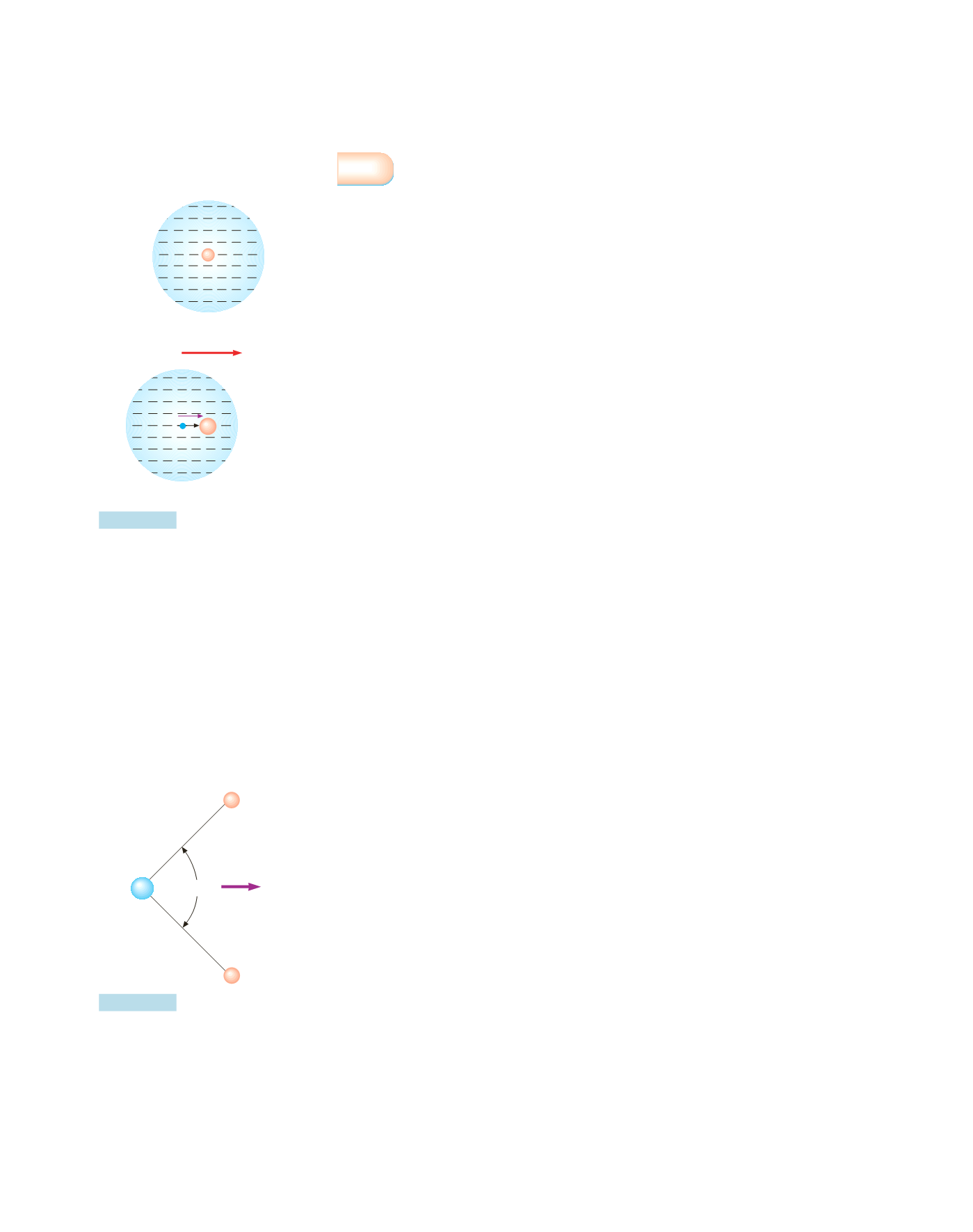
In un atomo in condizioni normali e in assenza di campo elettrico esterno la di-
stribuzione degli elettroni è in media simmetrica rispetto al nucleo: essa viene rap-
presentata, figura 4.40a, come una nube di carica negativa che occupa una zona
intorno al nucleo di raggio pari alle dimensioni dell’atomo (~10
–10
m); il centro di
massa della carica negativa coincide con il nucleo positivo.
Sotto l’azione di un campo elettrostatico
E
, figura 4.40b, il centro (di massa)
della nube negativa subisce uno spostamento in verso contrario al campo, il nu-
cleo in senso concorde al campo e si raggiunge una posizione di equilibrio in cui
questo effetto è bilanciato dall’attrazione tra le cariche di segno opposto. Detta
x
la distanza tra i centri delle cariche ovvero
x
il vettore che va dal centro della carica
negativa al nucleo, ha senso definire il
momento di dipolo elettrico
di questa con-
figurazione come
p
a
=
Ze
x
.
Possiamo quindi affermare che un atomo acquista un
momento di dipolo elettrico
microscopico
p
a
,
indotto
dal campo elettrostatico
E
, a questo parallelo e concorde;
l’effetto cessa quando si annulla il campo. Il fenomeno si chiama
polarizzazione elet-
tronica
.
Come abbiamo accennato alla fine del paragrafo 2.7 esistono delle sostanze le
cui molecole presentano un
momento di dipolo intrinseco
: si tratta di molecole polia-
tomiche formate da specie atomiche diverse (H
2
O, NH
3
) in cui la distribuzione
delle cariche è tale che il centro delle cariche negative non coincide con il centro
delle cariche positive, figura 4.41. In assenza di campo elettrostatico esterno, fi-
gura 4.42a, i dipoli molecolari sono orientati a caso, per via degli urti dovuti al
moto di agitazione termica che distruggono eventuali configurazioni ordinate do-
vute alle interazioni tra dipoli. Quando si applica un campo
E
, su ciascuno dei di-
poli elettrici di momento
p
0
agisce il momento delle forze (2.49) che ne causa un
orientamento con il campo elettrostatico soltanto parziale perché disturbato
dall’agitazione termica, figura 4.42b. Il grado di allineamento aumenta al dimi-
nuire della temperatura e all’aumentare dell’intensità del campo elettrostatico
esterno.
Anche questo meccanismo, che prende il nome di
polarizzazione per orienta-
mento
, porta al risultato che ogni molecola acquista un
momento di dipolo elettrico me-
dio
<
p
> microscopico parallelo al campo elettrostatico
E
, figura 4.42b.
Nella nota alla fine del capitolo 4 vengono esaminati entrambi i meccanismi di
polarizzazione per i gas.
4.7
+
+
p
a
= 0
(a)
(b)
p
a
=
Ze
x
E
p
x
_
_
+
+
H
O
H
p
0
105°
Momento di dipolo elettrico
Polarizzazione di un atomo sot-
toposto all’azione di un campo
elettrostatico.
Figura 4.40
Struttura elettrica della moleco-
la di acqua.
Figura 4.41
















