6 . 2
Cosa sono gli enantiomeri?
169
sti inorganici e di pochi semplici composti organici, la stragrande maggioranza delle
molecole nel mondo biologico mostra questo tipo di isomeria, compresi i carboidrati
(Capitolo 16), i lipidi (Capitolo 18), gli amminoacidi e le proteine (Capitolo 17) e gli
acidi nucleici (DNA e RNA, Capitolo 19). Inoltre, circa la metà dei farmaci attualmente
in uso è caratterizzata da questo tipo di isomeria.
Come esempio di molecola che esibisce enantiomeria, esaminiamo il 2-butanolo;
focalizziamo la nostra attenzione sul carbonio 2 di questa molecola, il carbonio che
porta il gruppo
¬
OH.
Ciò che rende questo carbonio interessante è che esso presenta
quattro gruppi differenti legati a sé. La causa più comune di enantiomeria tra le mole-
cole organiche è la presenza di un carbonio legato a quattro gruppi differenti.
2-Butanolo
OH
ƒ
CH
3
CHCH
2
CH
3
i quattro “gruppi” differenti
legati a questo atomo di
carbonio sono
¬
H,
¬
OH,
¬
CH
3
e
¬
CH
2
CH
3
La formula di struttura che abbiamo appena disegnato non mostra la forma del
2-butanolo, cioè, l’orientamento dei suoi atomi nello spazio. Per fare ciò, dobbiamo
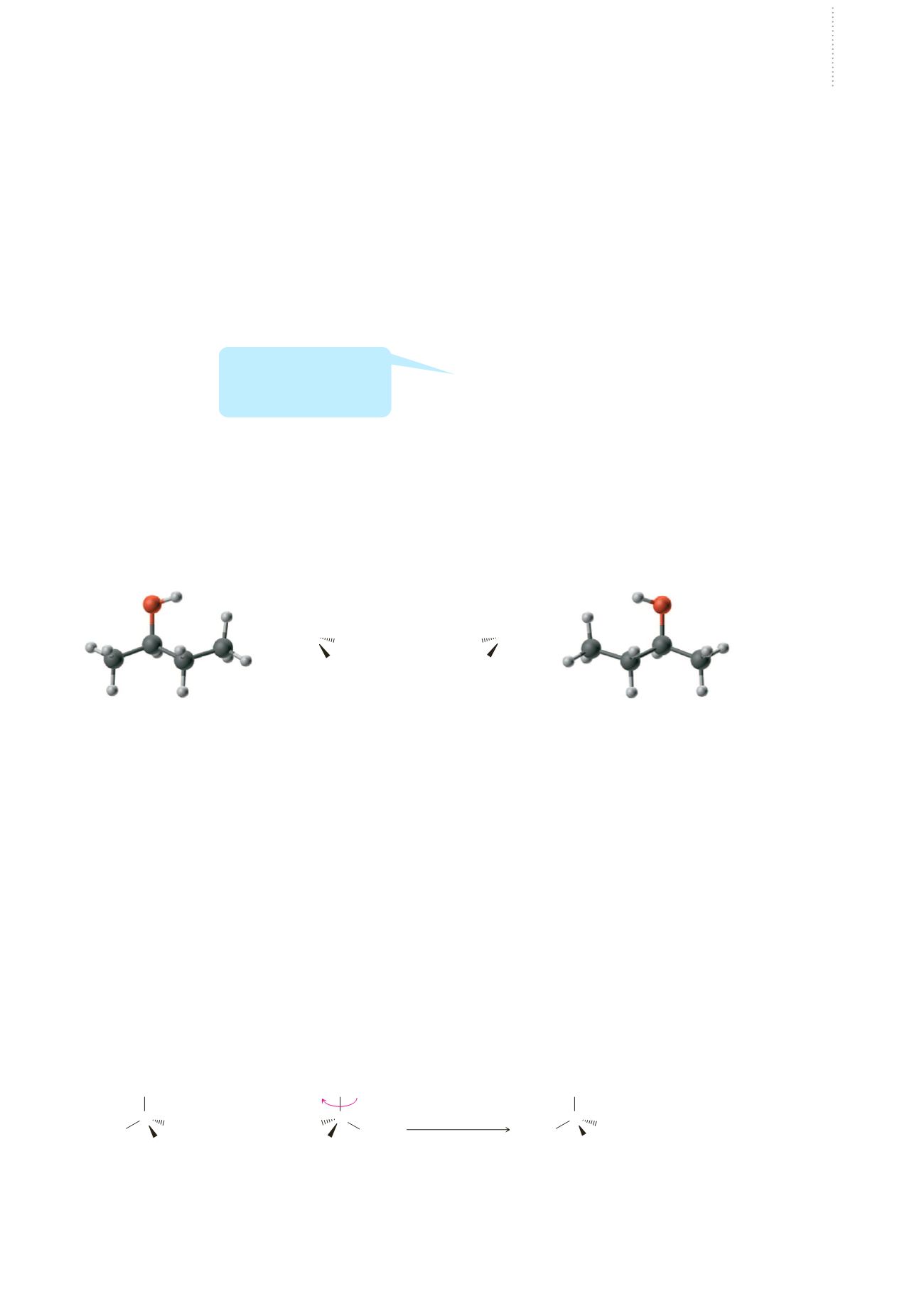
considerare la molecola come un oggetto tridimensionale. A sinistra dell’immagine
che segue, troviamo un modello a sfere e bastoncini del 2-butanolo e una formula
prospettica di quella che noi chiamiamo la “molecola originale”. In questa rappresen-
tazione, i gruppi
¬
OH e
¬
CH
3
legati al carbonio 2 sono nel piano del foglio; l’
¬
H è
dietro il piano e il gruppo
¬
CH
2
CH
3
è davanti a esso.
Originale
OH
ƒ
C
√
CH
2
CH
3
H
H
3
C
ƒ
C
√
CH
3
CH
2
H
CH
3
HO
Immagine speculare
A destra dell’immagine c’è l’immagine speculare della molecola originale. Ogni
molecola, come, del resto, ogni oggetto nel mondo che ci circonda, ha un’immagine
speculare. La domanda che dobbiamo porci è la seguente: “qual è la relazione tra l’ori-
ginale del 2-butanolo e la sua immagine speculare?” Per rispondere a questa domanda,
devi immaginare di prendere l’immagine speculare e di muoverla nello spazio in tutti i
modi possibili. Se, spostando l’immagine speculare, riesci a farla coincidere esattamen-
te con l’originale, nel senso che tutti i legami, gli atomi e ogni altro dettaglio corrispon-
dono, allora le due molecole sono
sovrapponibili
. In questo caso, l’immagine speculare
e l’originale rappresentano la stessa molecola; esse sono soltanto orientate in modo
differente nello spazio. Se, invece, per quanto tu possa ruotare l’immagine speculare
nello spazio, non riesci a farla coincidere con l’originale con tutti i dettagli che corri-
spondano, allora le due molecole sono
non sovrapponibili
, cioè, sono molecole diverse.
Il punto chiave è che un oggetto o è sovrapponibile alla propria immagine specu-
lare o non lo è. Osserviamo ora il 2-butanolo e la sua immagine speculare: “sono o non
sono sovrapponibili”?
Le immagini seguenti illustrano una maniera per vedere che l’immagine specula-
re del 2-butanolo non è sovrapponibile alla molecola originale:
ruota intorno al
legame C
¬
OH di 180°
H
3
C
C
OH
CH
2
CH
3
H
Molecola
originale
H
3
C
C
OH
H
CH
2
CH
3
CH
3
C
OH
H
3
CH
2
C
H
Immagine speculare
della molecola originale
Immagine speculare
ruotata di 180°
180
°


