Capitolo 36 |
Paraparesi spastiche ereditarie
550
proteina PLP1 e la sua isoforma DM20 sono
abbondantemente espresse negli oligodendroci-
ti e rappresentano circa il 50% del totale delle
proteine costituenti la mielina nel sistema ner-
voso centrale. I disordini legati alla PLP1 rap-
presentano un continuum che va dalla malattia
di Pelitzeus-Mezbacher (PMD) con grave com-
promissione cerebrale sino alla SPG2. Possono
essere osservate anche variazioni intrafamiliari
del fenotipo.
L’SPG2 può presentarsi come paraplegia spastica
pura o complicata. I sintomi più frequentemente
osservati sono il nistagmo e l’atassia. Una distin-
zione chiara sui criteri obiettivi non può essere
tracciata tra forme complicate di paraparesi spasti-
ca e forme non gravi di PMD. La durata media di
vita nell’SPG2 non è ridotta.
Alla RM del cranio i pazienti con SPG2 possono
presentare aree di alterato segnale nelle immagi-
ni T2-pesate o una leucoencefalopatia diffusa (si
veda il Capitolo 37).
■
Un algoritmo per i test genetici
nelle paraparesi spastiche ereditarie
L’EFNS (European Federation of Neurological
Society) nel 2010 ha proposto le linee guida per
la diagnosi di PSE, che rappresentano un ovvio,
grande aiuto per il neurologo che si trovi a valuta-
re un paziente con paraparesi spastica. Ciò nono-
stante, in presenza di un sospetto di PSE, l’attenta
osservazione di fenotipo, decorso clinico e mo-
dalità di trasmissione della patologia rappresenta
la “guida” migliore nella scelta del test genetico.
Va sottolineato che identificare una mutazione
genetica responsabile di PSE non indica né l’età
alla quale i sintomi compariranno né la severità
della patologia. In generale, il counseling geneti-
co nelle PSE deve considerare la modalità di tra-
smissione di quella forma specifica, la frequenza
di mutazioni spontanee nelle forme dominanti, il
grado di penetranza della mutazione e la variabi-
lità clinica. Dalla letteratura si evince che circa il
12% dei soggetti con forme apparentemente spo-
radiche di PSE presenta una mutazione compati-
bile con una ereditarietà autosomica dominante.
Il counseling genetico deve infine considerare
anche il fenomeno dell’anticipazione, che è sta-
to osservato, seppur in una minoranza di casi, in
soggetti affetti da SPG4 e SPG3A. Nella Figura
36.3 viene riportato il “percorso” consigliato da
intraprendere per formulare una corretta diagnosi
genetica di PSE.
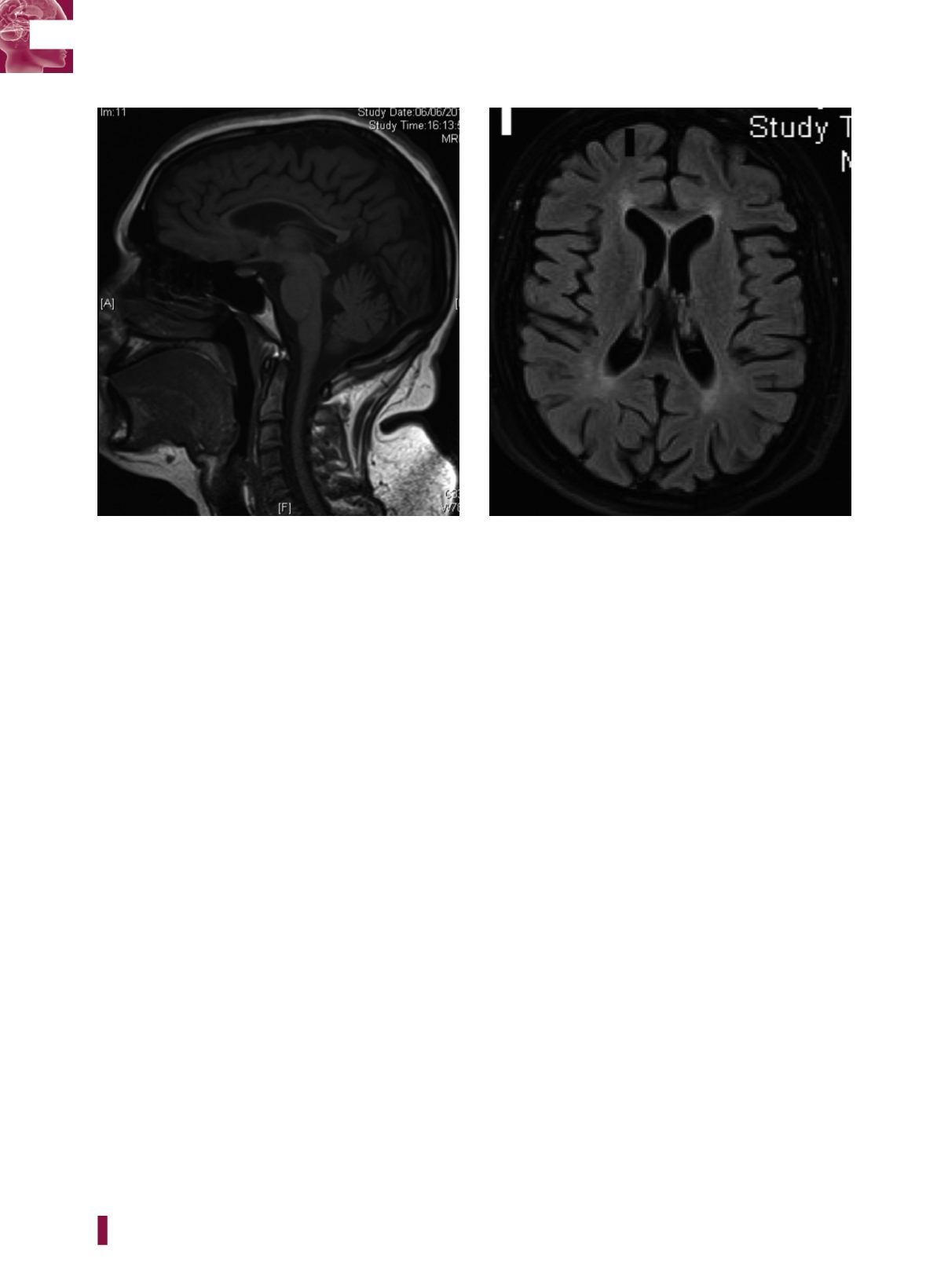
Figura 36
.
2
| (A) Sezione sagittale, immagine T1-pesata. Aspetto marcatamente sottile del corpo calloso. Spazi sottotentoriali, in
particolare quelli nella porzione superiore del verme cerebellare, con aspetto moderatamente ampliato. (B) RM del cranio. Sezione
assiale, immagine T1. Tenue iperintensità nelle sequenze tardive a carico della sostanza bianca periventricolare adiacente a corni
occipitali, celle medie e corni frontali, con risparmio delle fibre U.
A
B


