
C A P I TO LO 8
Alcoli, eteri e tioli
232
FIGURA 8.3
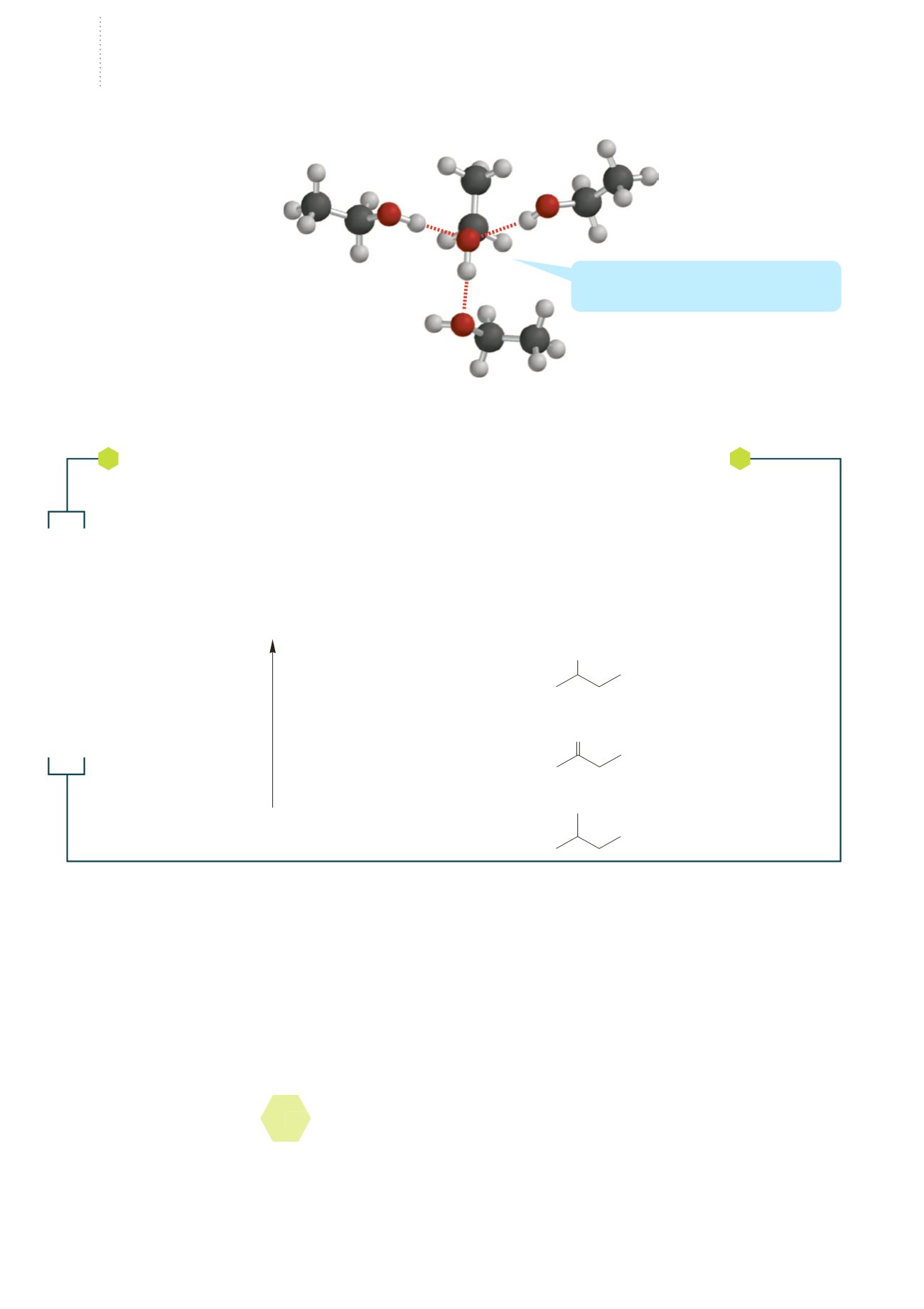
L’associazione delle molecole di
etanolo allo stato liquido. Ogni
O—H può partecipare ad un
massimo di tre legami idrogeno
(uno mediante l’idrogeno e due
mediante l’ossigeno).
δ
–
δ
–
δ
–
δ
–
δ
+
δ
+
δ
+
questa molecola è mostrata partecipare a tre
legami idrogeno (mostrati come
]]]]]]]]]
)
: due
mediante l’ossigeno ed uno mediante l’idrogeno
Come prevedere i punti di ebollizione relativi di composti con peso
molecolare simile
COME FARE
8.2
(a)
Cerca di individuare quelle caratteristiche che fanno aumentare il punto di ebollizione di un composto, quali una
maggiore polarità, la capacità di formare legami idrogeno con altre molecole (valido per composti contenenti
legami N—H o O—H), una maggiore super"cie molecolare.
(b)
Il punto di ebollizione solitamente segue questo andamento:
composti polari che sono
sia
donatori
sia
accettori
di legami idrogeno
Esempi
composti non polari
composti polari che non
possono stringere legami idrogeno
o che possono essere solo donatori
o accettori di legami idrogeno,
ma non entrambi
OH
p.e.
=
98°C
p.e.
=
28°C
Punto di ebollizione
più alto
Punto di ebollizione
più basso
p.e.
=
80°C
O
mentare del peso molecolare. (Confronta, per esempio, i punti di ebollizione di etanolo,
1-propanolo, 1-butanolo e 1-pentanolo).
Gli alcoli sono molto più solubili in acqua rispetto agli alcani, agli alcheni e agli alchini
di pari peso molecolare. L’aumento della loro solubilità è dovuto ai legami idrogeno tra
le molecole di alcol e di acqua. Metanolo, etanolo e 1-propanolo sono solubili in acqua in
tutte le proporzioni. All’aumentare del peso molecolare, le proprietà fisiche degli alcoli di-
ventano più simili a quelle degli idrocarburi di simile peso molecolare. Gli alcoli a più alto
peso molecolare sono molto meno solubili in acqua a causa dell’aumento di dimensione
della parte idrocarburica della molecola.
8.2
Quali sono le reazioni caratteristiche degli alcoli?
In questo paragrafo studieremo l’acidità e la basicità degli alcoli, la loro disidratazione ad
alcheni, la loro trasformazione in alogenuri alchilici e la loro ossidazione ad aldeidi, cheto-
ni o acidi carbossilici.
















