
3 . 5
Proprietà periodiche degli elementi
Le proprietà chimiche e fisiche degli elementi sono determinate dalle loro
configurazioni elettroniche e sono quindi funzione periodica del numero ato-
mico. Alcune di queste proprietà, come le dimensioni atomiche, l’energia di io-
nizzazione e l’affinità elettronica, saranno presentate in questo capitolo e verrà
inoltre spiegato qualitativamente come queste proprietà variano lungo un
gruppo o un periodo della tavola periodica.
3.5.1 Dimensioni atomiche
La determinazione delle dimensioni di un atomo non è un problema di fa-
cile risoluzione poiché la nube elettronica di un atomo non ha dei contorni esat-
tamente definiti. Inoltre il raggio di un atomo può dipendere dal numero e dal
tipo di atomi con cui è legato in un determinato composto.
Il
volume atomico
di un elemento può essere calcolato dividendo il suo peso
atomico per la densità. Nel 1870 L. Meyer diagrammando i valori dei volumi
atomici dei vari elementi in funzione del numero atomico rilevò una variazione
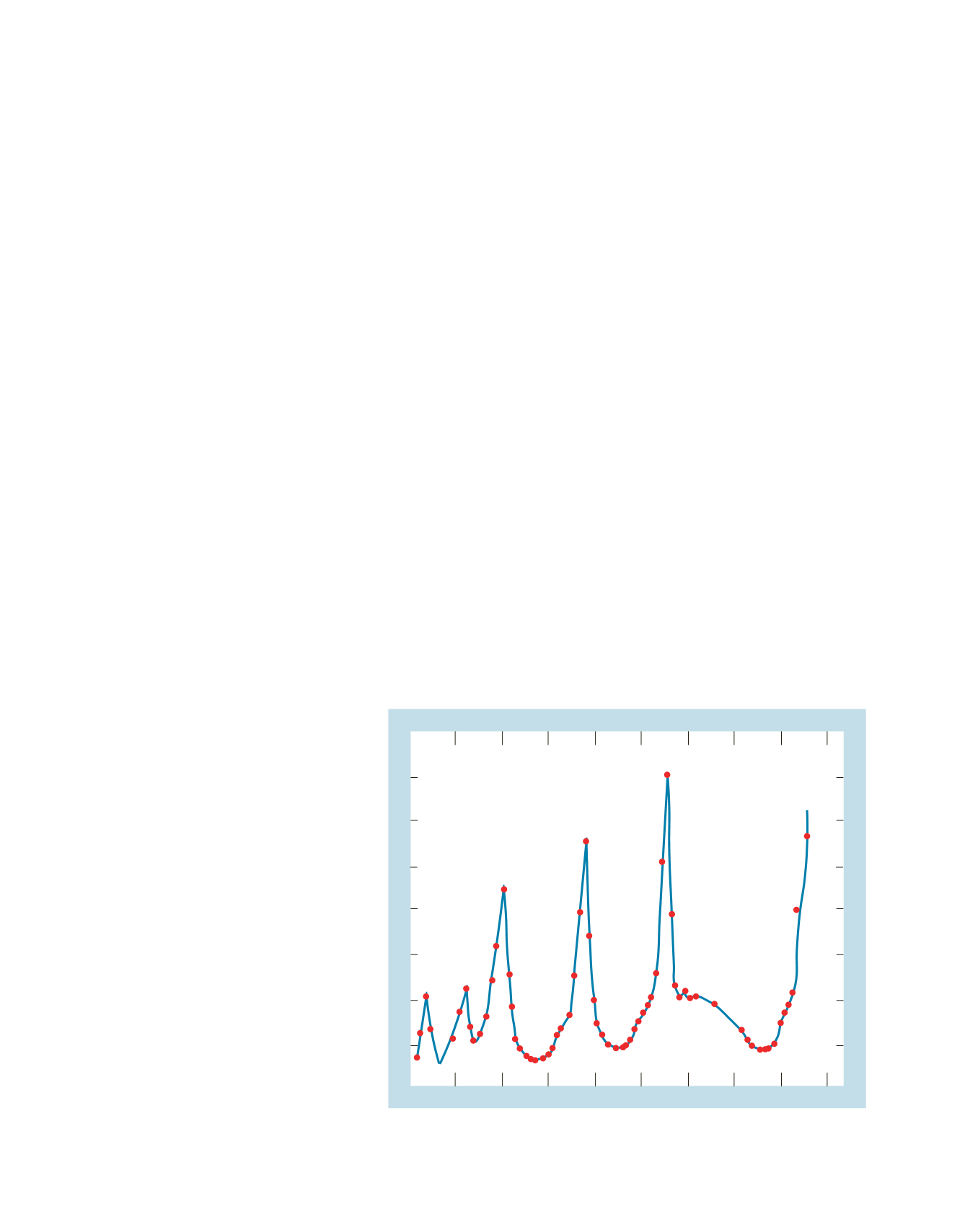
periodica di questa grandezza. Come mostrato nella Figura 3.3, i volumi atomici
risultano massimi per i metalli alcalini e hanno dei valori minimi per gli elementi
centrali dei vari periodi. Il progressivo aumento dell’altezza dei massimi indica
che il volume atomico degli elementi che appartengono allo stesso gruppo cre-
sce al crescere del numero atomico.
Il volume atomico così calcolato è un’indicazione solo qualitativa delle di-
mensioni atomiche. Infatti la densità di un elemento dipende dalla temperatura
e dalla sua struttura cristallina, per cui un elemento quale il carbonio, che può
esistere sotto diverse forme cristalline (es. grafite e diamante), dovrebbe presen-
tare paradossalmente valori diversi delle sue dimensioni.
74
Capitolo 3 Il sistema periodico
10 20 30 40 50 60 70 80 90
B
Co
Rh
Os
Li
Na
K
Rb
Cs
70
60
50
40
30
20
10
0
Numero atomico
Volume atomico (cm
3
/mole)
Figura 3.3
Dipendenza del volume atomico degli ele-
menti dal numero atomico.
















